Cómo encontrar la reacción redox

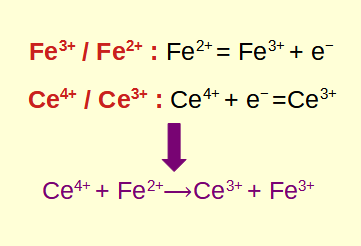

Las reacciones redox, abreviatura de reacciones de oxidación-reducción, son procesos químicos fundamentales que implican la transferencia de electrones entre reactivos. Comprender cómo identificar y calcular reacciones redox es crucial en los campos de la química y la biología. En esta publicación de blog, exploraremos los conceptos básicos de las reacciones redox, aprenderemos cómo identificarlas, profundizaremos en los cálculos involucrados y exploraremos sus aplicaciones prácticas.
Comprender los conceptos básicos de las reacciones redox
Las reacciones redox ocurren cuando hay una transferencia de electrones entre dos especies. Una especie pierde electrones (sufre oxidación) mientras que la otra especie gana electrones (sufre reducción). Esta transferencia de electrones está impulsada por una diferencia en la electronegatividad de los átomos involucrados.
La especie oxidada se conoce como agente reductor porque dona electrones, mientras que la especie reducida se llama agente oxidante porque acepta electrones. Es importante tener en cuenta que las reacciones redox siempre implican tanto oxidación como reducción, de ahí el nombre.
Importancia de las reacciones redox
Las reacciones redox desempeñan un papel crucial en diversos procesos químicos y biológicos. Están involucrados en la producción de energía, la corrosión, la síntesis de sustancias químicas e incluso el funcionamiento de nuestro propio cuerpo. Por ejemplo, el proceso de fosforilación oxidativa, que ocurre en las mitocondrias de nuestras células, se basa en reacciones redox para producir ATP, la moneda energética universal de las células.
Ejemplos comunes de reacciones redox
Echemos un vistazo a algunos ejemplos comunes de reacciones redox:
Combustión: Cuando una sustancia reacciona con el oxígeno para producir calor y luz, se trata de una reacción redox. Por ejemplo, la quema de madera o la combustión de gasolina en el motor de un coche.
Oxidación: El proceso de oxidación implica la oxidación del hierro en presencia de oxígeno y agua. El hierro pierde electrones y forma óxido de hierro (III).
Fotosíntesis: Durante la fotosíntesis, las plantas convierten el dióxido de carbono y el agua en glucosa y oxígeno, con la ayuda de la luz solar. Este proceso implica la reducción del dióxido de carbono y la oxidación del agua.
Identificación de reacciones redox
Para identificar una reacción redox, necesitamos reconocer las sustancias que están sufriendo oxidación y reducción. Aquí hay algunos pasos clave que nos ayudarán a identificar reacciones redox rápidamente:
Reconocer la oxidación y la reducción: buscar cambios en los estados de oxidación o la pérdida/ganancia de electrones. Si el estado de oxidación de un elemento aumenta, se está oxidando, mientras que una disminución del estado de oxidación indica una reducción.
Determinación del número de oxidación: el número de oxidación es un concepto utilizado para determinar la distribución de electrones en un compuesto o ion. Nos ayuda a identificar el cambio de estados de oxidación durante una reacción redox.
Identificar reacciones redox rápidamente: un método eficaz para identificar reacciones redox es buscar la presencia de ciertos elementos o compuestos que se sabe que sufren reacciones redox. Por ejemplo, el peróxido de hidrógeno (H2O2) es un agente oxidante común, mientras que sustancias como el borohidruro de sodio (NaBH4) son agentes reductores.
Calcular reacciones redox
Una vez que hayamos identificado una reacción redox, podemos proceder a calcularla. Así es cómo:
Encontrar las medias reacciones: divida la reacción redox en dos medias reacciones, una que represente la oxidación y la otra que represente la reducción. Esto ayuda a equilibrar la ecuación más adelante.
Equilibrio de la reacción redox: equilibre el número de átomos en cada lado de la ecuación ajustando los coeficientes. Es esencial equilibrar tanto la masa como la carga cuando se trata de reacciones redox.
Cálculo de la reacción redox general: combine las semireacciones equilibradas, asegurándose de que la cantidad de electrones ganados en la reducción coincida con la cantidad de electrones perdidos en la oxidación.
Conceptos avanzados en reacciones redox
Para profundizar nuestra comprensión de las reacciones redox, exploremos algunos conceptos avanzados:
Determinación de la espontaneidad de las reacciones redox: la espontaneidad de una reacción redox se puede determinar utilizando el concepto de potencial redox. Si el potencial redox es positivo, la reacción es espontánea, lo que indica una mayor probabilidad de que ocurra.
Encontrar el coeficiente de reacciones redox: Los coeficientes en una reacción redox equilibrada representan el número relativo de moles de cada especie involucrada. Estos coeficientes son cruciales para los cálculos estequiométricos.
Comprender el papel de los electrones en las reacciones redox: los electrones son los portadores de carga en las reacciones redox. Viajan del agente reductor al oxidante, facilitando la transferencia de energía.
Aplicaciones prácticas de las reacciones redox
Las reacciones redox tienen aplicaciones prácticas en diversos dominios. Exploremos algunos ejemplos:
Reacciones redox en la vida cotidiana: el proceso de respiración en nuestro cuerpo se basa en reacciones redox para convertir la glucosa en energía. Además, las baterías que utilizamos a diario, como las alcalinas y las de iones de litio, funcionan en base a reacciones redox.
Aplicaciones industriales de las reacciones redox: las reacciones redox son cruciales en procesos industriales como la extracción de metales, la galvanoplastia y el tratamiento de aguas residuales. Ayudan a eliminar contaminantes nocivos y convertirlos en sustancias menos tóxicas.
Reacciones redox en sistemas biológicos: en el cuerpo humano, las reacciones redox están involucradas en varios procesos biológicos, incluido el metabolismo, la desintoxicación y las respuestas inmunes. Sin embargo, las reacciones redox excesivas pueden provocar estrés oxidativo, que puede dañar las células y contribuir a la aparición de enfermedades.
Lea también
- Reacción de Knoevenagel
- Ejemplo de reacción dependiente de la luz
- Reacción endotérmica
- Reacción de sustitución nucleofílica
- Ejemplo de reacción de síntesis
- Reacción fotoquímica
- Ejemplo de reacción endergónica
- Ejemplo de reacción de primer orden
- Ejemplo de reacción independiente de la luz.
- reacción de kolbe

Hola,
Soy Aditi Ray, una PYME de química en esta plataforma. Completé mi graduación en Química de la Universidad de Calcuta y un posgrado de la Universidad Techno India con especialización en Química Inorgánica. Estoy muy feliz de ser parte de la familia Lambdageeks y me gustaría explicar el tema de una manera simplista.
Conectémonos a través de LinkedIn-https://www.linkedin.com/in/aditi-ray-a7a946202

Hola compañero lector,
Somos un equipo pequeño en Techiescience y trabajamos duro entre los grandes jugadores. Si te gusta lo que ves, comparte nuestro contenido en las redes sociales. Su apoyo hace una gran diferencia. ¡Gracias!